细胞膜运转领域三位科学家分享2013年诺贝尔生理医学奖
根据诺贝尔奖委员会网站消息,2013诺贝尔生理学或医学奖于北京时间7日17时30分揭晓:James E. Rothman,Randy W. Schekman 与 Thomas C. Südhof 三人分享2013年诺贝尔生理学或医学奖(The 2013 Nobel Prize in Physiology or Medicine)。
获奖理由是“发现细胞内的主要运输系统——囊泡运输的调节机制”("for their discoveries of machinery regulating vesicle traffic, a major transport system in our cells")。
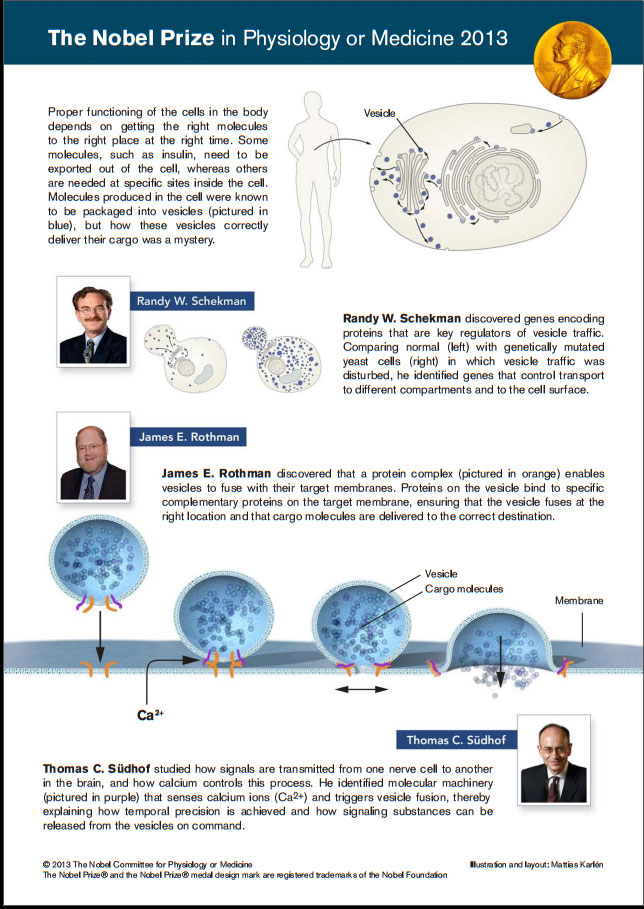
2013年诺贝尔生理学或医学奖授予了三位解开细胞如何组织其运输系统之谜的科学家。每个细胞如同一座工厂,制造和输出着各类分子比如胰岛素产生后释放到血液中,而被称为神经传递素的化学信号则通过一个神经细胞传递到另外一个神经细胞。这些分子都被运输到细胞周围的被称为囊泡的小“包裹”中。这次获奖的三位科学家解开了调控运输物在正确时间投递到细胞中正确位置的分子原理。
Randy Schekman 发现了囊泡传输所需的一组基因;James Rothman 阐明了囊泡是如何与目标融合并传递的蛋白质机器;Thomas Südho f则揭示了信号是如何引导囊泡精确释放被运输物的。通过研究,Rothman, Schekman 和 Südhof 揭开了细胞物质运输和投递的精确控制系统的面纱。该系统的失调会带来有害影响,并可导致诸如神经学疾病、糖尿病和免疫学疾病等的发生。
细胞内物质输运是如何实现的?
正如在一个繁忙的大型港口,你必须要有一套体系来确保你的货物会在规定的时间被配送到规定的位置,细胞也是一样。细胞内有各种复杂的细胞器,它们面临的问题是相似的:细胞会产生出各种不同的分子,如荷尔蒙,神经传递素,细胞活素以及酶,它们必须被传递至细胞内不同的位置上,或者需要被精确地在正确的时间转运至细胞外部。在这一过程中,时间和地点的正确是最关键的。这就要依赖于囊泡的作用,这是一些微小的小泡结构,外部有膜包裹,它们负责在各细胞器之间运输细胞内部的“货物”,或是通过与细胞膜的融合从而向细胞外部释放细胞内产生的物质。这一机制至关重要,如它控制着神经传递素的传递,后者是激发生物体神经系统反应的触发开关;又或者在新陈代谢方面,它控制着荷尔蒙的分配传递。那么这些囊泡结构究竟是如何能确保运输的时间和地点正确性的呢?
交通堵塞背后的基因控制机制
早在上世纪的1970年代,Randy Schekman便被细胞如何调节其内部输运机制深深吸引并投身此项研究,并试图利用酵母菌作为模型样本来研究其背后的基因机制。在基因筛选中,他找到一些显示出输运机制缺陷的酵母菌细胞,其表现就像是一个缺乏指挥协调而一片混乱的公共交通系统,其内部囊泡堆积在细胞内的部分区域。他发现造成这种囊泡发生“交通堵塞”的原因是基因层面的,并据此顺藤摸瓜找到了其背后的基因机制。他找到了3组不同的基因对这一细胞运输机制产生作用,从而改变并大大加深了我们对细胞如何规范其内部输运系统的认识。
精确对接
James Rothman同样对细胞输运机制感到好奇。在上世界80~90年代期间,Rothman正开展对哺乳动物细胞囊泡输运机制的研究,他发现一种蛋白质可以让囊泡实现与其目标细胞膜的对接和融合。在融合过程中,囊泡上的蛋白质和细胞膜上的蛋白质相互结合,就像分开的拉链相互咬合一样。这类蛋白质有很多种,并且只有当合适的配对出现时才会发生融合,这就确保了“货物”只会被运输到设定的位置上而不会出现错误。这一机制不管是在内部细胞器之间的运输,还是向外的运输过程中都会起作用。
随后的研究发现,Schekman在酵母菌细胞内所发现的部分基因正是产生Rothman在哺乳动物细胞内发现的蛋白质的背后机制,这揭示了一项细胞输运体系内古老的进化起源。至此,这两位科学家的研究工作描绘了细胞输运体系的关键环节。
时间就是一切
Thomas Südhof对大脑内神经细胞是如何相互之间进行沟通感兴趣。这种传递信息的物质被称为神经传递素,这种特殊分子正是由囊泡负责运输至神经细胞的细胞膜上并借助融合机制向外释放的。这正是Rothman 和Schekman所发现的机制。然而这些囊泡只有在其所在的神经细胞向其“邻居”发送信号之后才会被允许释放它们运载的“货物”。这种精确的时机把握究竟是如何实现的?
科学家们此前便已经知道钙离子参与了这一过程,在上世纪90年代,Südhof便开始在神经细胞中寻找对钙离子敏感的蛋白质。最终他识别出一种分子机制,其会对注入的钙离子做出反应,并控制邻近的蛋白质迅速让囊泡与神经细胞的外部细胞膜相结合。于是“拉链”打开了,信号物质被释放出去。Südhof的发现解释了这种细胞传输的时间精确性是如何实现的,以及囊泡中的物质是如何实现受控地释放。
囊泡输运机制与疾病过程
今年的3位诺奖获奖科学家发现了细胞生理学过程中的一项关键过程。他们的工作揭示了细胞内部和外部的输运体系是如何达成时间与位置上的精确性的。在细胞中,不管是酵母菌还是人类,不管高等生物还是低等生物,它们体内的囊泡输运以及细胞膜融合机制都遵循相同的基本原理。这一体系对于一系列的生理过程而言都至关重要,从大脑信号的传递,到荷尔蒙的释放,再到免疫细胞活素。但当发生疾病时,细胞内的囊泡输运机制会出现问题,这当中包括一些神经系统和免疫系统疾病。离开这一堪称完美的控制机制,细胞将陷于混乱。